辉瑞股票交易策略:2021.12.16 从技术图形上看,股价经过短期震荡,已经突破前期交易区间50美元-55美元之间,股价收于58美元之上,建议短线交易在20日均线上方多单持有,中长线在60日均线上方多单持有。如果股价跌破55美元,可能出现向下调整的行情。出场顺序,短线交易股价跌破20日均线转空,中长线交易跌破60日均线转空。从基本面来看,股价估值合理,营收持续保持增长,值得长期持有。
历史预测记录:
2021.12.16 中国国家药监局(NMPA)最新公示,辉瑞(Pfizer)引进的抗感染新药硫酸艾沙康唑胶囊的上市申请已获得批准。根据辉瑞公司早前发布的新闻稿,艾沙康唑(Cresemba)是治疗成人侵袭性曲霉病和毛霉菌病的一种新颖的抗真菌药。
2021.12.15 SVB Leerink维持辉瑞评级为市场持平,最新目标价为56美元。
2021.12.13 从技术图形上看,股价高位震荡,暂无趋势性行情,近期波动区间为50美元-54美元之间,建议短线交易在20日均线上方多单持有,中长线在60日均线上方多单持有。如果股价跌破50美元,可能出现向下调整的行情。出场顺序,短线交易股价跌破20日均线转空,中长线交易跌破60日均线转空。从基本面来看,股价估值合理,营收持续保持增长,值得长期持有。
2021.12.05 从技术图形上看,股价处于上涨趋势中,建议短线交易在20日均线上方多单持有,中长线在60日均线上方多单持有。如果股价跌破50美元,可能出现向下调整的行情。出场顺序,短线交易股价跌破20日均线转空,中长线交易跌破60日均线转空。从基本面来看,股价估值合理,营收持续保持增长,值得长期持有。
辉瑞公司(纽约证券交易所代码:PFE)于11月02日发布2021年第三季度报告,公司截至2021年10月3日,营业收入240.9亿美元,同比去年增加134.45%,净利润81.47亿美元,同比去年增加454.59%,稀释后基本每股收益 1.42美元。
上调2021年全年指引(4)收入在810亿美元到820亿美元之间,调整后稀释每股收益(3)至4.13美元至4.18美元的区间,反映出中点的同比增长率分别为94%和84%。
预计2021年Comirnaty的收入约为360亿美元(1),预计将在2021财年交付23亿剂。
提高调整后稀释每股收益指引的中点(3)不包括Comirnaty (1)至2.60美元至2.65美元的区间。
于11月17日宣布,Frank D的阿梅里奥将从辉瑞公司首席财务官兼全球供应执行副总裁的职位上退休,此前他在辉瑞公司工作了近15年。辉瑞已开始从外部寻找新的首席财务官,达梅里奥已同意在这一过程中留在董事会,并在过渡期间担任咨询职务。
最近的显著发展(自2021年7月28日以来)
Abrilada(阿达木单抗-AFZB,生物仿制药)–2021年9月,辉瑞公司从Reflections B538-12研究中获得了积极的结果,该研究评估了Abrilada治疗与其参考产品Humira之间的多种转换®在患有中度至重度类风湿关节炎的成年患者中,这两种药物都使用甲氨蝶呤。该研究通过在两种药物治疗之间多次转换的患者中证明药物动力学的等效性,达到了其主要终点。两臂的安全性和免疫原性相似。辉瑞公司计划最早于2023年7月1日在美国推出不含柠檬酸盐的Abrilada,这是根据与该鼻祖公司的协议条款。
Chantix –2021年9月,辉瑞自愿在美国召回所有批次的Chantix,原因是存在达到或超过FDA临时可接受摄入量限制的亚硝胺,N-亚硝基-伐伦尼克林。亚硝胺在水和食物中很常见,每个人都会接触到一定水平的亚硝胺。如果人们长时间暴露在超过可接受水平的物质中,这些杂质可能会增加患癌症的风险。戒烟对健康的好处超过了瓦伦尼克林中的亚硝胺杂质理论上潜在的致癌风险。
2021年8月,辉瑞公司宣布,Jade Dare(B7451050)是一项为期26周的随机,双盲,双模拟,主动对照,多中心3期研究,评估阿博替尼200mg与Dupilumab300mg在成年患者中进行中度至重度特应性皮炎的本底局部治疗,达到了其共同主要和关键的次要疗效终点。该研究表明,在每项评估的疗效指标中,阿博替尼在统计学上都优于杜匹鲁单抗,其安全性与先前的研究一致。
2021年9月,辉瑞宣布,英国药品和医疗保健产品监管局已授予Cibinqo的上市许可,用于治疗12岁及以上的成人和青少年中的中度至重度AD,这些人是系统性治疗的候选人。Cibinqo在英国获得许可,推荐剂量为100毫克和200毫克。
2021年10月,辉瑞公司宣布,欧洲药品管理局的人用药品委员会通过了一项积极的意见,建议将100毫克和200毫克剂量的阿博替尼用于上市许可,以治疗成人中的中度至重度AD,这些人可能需要进行全身治疗。
Comirnaty(BNT162b2,新冠病毒疫苗,mRNA)
2021年9月,辉瑞和BioNTech宣布了BNT162b2的2/3期试验结果,该结果显示,在5岁至11岁的儿童中,使用10克的两剂量方案,每隔21天给药,具有良好的安全性和强大的中和抗体反应,比12岁及以上人群使用的30克剂量更小的剂量。接受10克剂量免疫的参与者的抗体反应与辉瑞-BioNTech之前的一项研究中记录的16至25岁接受30克剂量免疫的人的抗体反应相似。考虑到安全性、耐受性和免疫原性,选择10克剂量作为5至11岁儿童的首选剂量。
2021年10月,辉瑞和BioNTech宣布了一项3期随机对照试验的结果,该试验评估了30克加强剂量的Comirnaty在10,000多名16岁及以上的人中的有效性和安全性。在该试验中,向先前接受了两次剂量系列的主要Comirnaty的个人施用加强剂量,将针对新冠病毒的疫苗保护恢复到第二次剂量后达到的高水平,与未接受加强剂量的人相比,显示出95.6%的相对疫苗效力。这是任何随机、对照的新冠肺炎疫苗强化试验的首个疗效结果。不良事件概况与该疫苗的其他临床安全性数据基本一致,没有发现新的安全隐患。
2021年8月,辉瑞和BioNTech宣布,根据全面的数据包,FDA批准了Comirnaty的Biologics License Application,用于在16岁及以上的个人中预防新冠病毒的两剂主要系列(每剂30克)其中包括来自3期试验的长期随访数据,在该试验中,在第二次接种后的6个月内观察到了该疫苗的高功效和安全性。Comirnaty是第一个获得FDA批准的新冠病毒疫苗,自2020年12月11日以来,该疫苗已在美国根据紧急使用授权向该患者人群提供。根据FDA于2021年5月10日批准的EUA,该疫苗仍可用于12至15岁的个人。(9).
2021年8月,辉瑞和BioNTech宣布向FDA提交补充生物制剂许可申请,以批准加强剂量(第三剂)Comirnaty,以预防16岁及以上的人的新冠病毒。SBLA包括一项3期临床试验的数据,该试验涉及306名18-55岁的参与者,他们在完成两剂初级方案后的4.8至8个月内接受了第三剂Comirnaty,中位随访时间为加强后的2.6个月。第三次给药后,SARS-CoV-2 50%中和效价是第二次给药后的3.3倍。反应原性的频率与给药后的两个主要系列相似或更好。不良事件概况与Comirnaty的其他临床数据总体上一致。
2021年9月,辉瑞和BioNTech宣布FDA授权紧急使用(9)针对65岁及以上的个人,18至64岁具有严重新冠肺炎高风险的个人,以及18至64岁经常在机构或职业中暴露于SARS-CoV-2的个人,加强剂量的Comirnaty。加强剂量应在主要系列完成后至少六个月进行给药,并且与主要系列中的剂量具有相同的配方和剂量强度。此外,在2021年10月,FDA授权紧急使用(9)向已完成不同授权新冠病毒疫苗的初级疫苗接种的合格个人提供加强剂量。异源加强剂量的合格人群和剂量间隔与用于初级疫苗接种的疫苗的加强剂量的授权人群和剂量间隔相同。
2021年10月,辉瑞和BioNTech宣布,FDA已授权BNT162b2用于紧急使用(9)适用于5岁至11岁的儿童。对于这一组人,疫苗将在两次剂量的方案中给药,每次10克剂量,间隔21天。FDA的决定基于一项2/3期随机对照试验的数据,该试验包括约4500名参与者(2268名来自原组,2379名来自补充安全组)。FDA疫苗及相关生物产品咨询委员会对该试验的结果进行了审查,该委员会以17票对0票、1票弃权的投票结果,建议FDA为该年龄段的疫苗授予EUA。下一步,美国疾病控制和预防中心的ACIP将开会讨论一项可能的建议,以便在5至11岁的儿童中使用和推广这种疫苗。这两家公司已经向世界各地的其他监管机构提交了这一年龄段的授权请求,其中包括EMA。
2021年10月,辉瑞和BioNTech宣布,美国政府根据现有的美国供应协议行使了其最终购买选择权,以购买5000万剂BNT162b2。这些额外的剂量旨在支持美国对儿科疫苗接种的准备,包括确保5岁以下儿童的疫苗,如果他们获得监管机构的授权。这使得目前根据该协议获得的剂量总数达到6亿,涵盖了成人、青少年和儿童的剂量。这些公司预计将在2022年4月30日之前交付所有这些剂量。
2021年11月,辉瑞与总部位于纽约的医疗保健投资公司Altaris Capital Partners,LLC达成协议,由Altaris购买Meridian Medical Technologies。Meridian于2011年被辉瑞收购,作为King Pharmaceuticals收购的一部分,自那时以来一直保持相对的运营自主权。Meridian的业务每年产生约3亿美元的收入,包括制造和分销美国国防部,紧急医疗服务,国土安全部,卫生部和国防部使用的医疗对策,以及用于紧急治疗过敏反应(包括过敏反应)的救援自动注射器。该交易预计将在未来几个月内完成,但需满足惯例成交条件,包括获得监管机构的批准。
辉瑞公司(纽约证券交易所代码:PFE)于11月02日发布2021年前三季度报告,公司截至2021年10月3日,营业收入576.5亿美元,同比去年增加90.75%,净利润185.9亿美元,同比去年增加123.58%,稀释后基本每股收益 3.27美元。
股票代码:PFE
公司名称:辉瑞公司
英文名称:Pfizer Inc.
公司网址: www.pfizer.com
员工人数:78500
联系电话:1-212-7332323
公司总裁:Frank A. D’Amelio
办公地址:235 East 42nd Street New York New York 10017
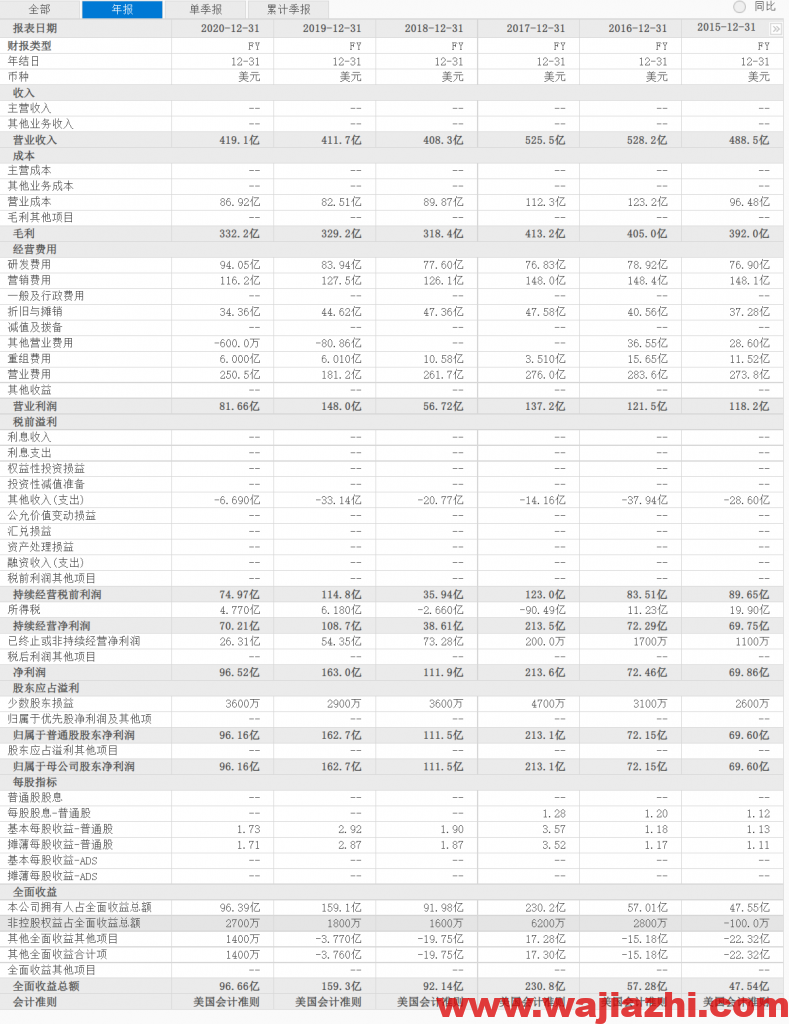
最近6年利润表
关于辉瑞:改变患者生活的突破
在辉瑞公司,我们运用科学和我们的全球资源,将疗法带给人们,从而延长并显著改善他们的生活。我们致力于为包括创新药物和疫苗在内的医疗保健产品的发现、开发和生产制定质量、安全和价值标准。每天,辉瑞的同事们都在发达市场和新兴市场开展工作,以推进健康、预防、治疗和治疗,挑战我们这个时代最令人恐惧的疾病。作为全球领先的创新生物制药公司之一,我们与医疗保健提供者,政府和当地社区合作,以支持和扩大在世界各地获得可靠,负担得起的医疗保健的机会。170多年来,我们一直在努力为所有依赖我们的人带来改变。我们经常发布可能是在我们的网站www.pfizer.com上对投资者很重要。此外,要了解更多信息,请访问我们的网站www.pfizer.com,并在Twitter上通过@pfizer关注我们 以及在Facebook.com/Pfizer上@Pfizer News、LinkedIn、YouTube和Like Us。
About Pfizer: Breakthroughs That Change Patients’ Lives
At Pfizer, we apply science and our global resources to bring therapies to people that extend and significantly improve their lives. We strive to set the standard for quality, safety and value in the discovery, development and manufacture of health care products, including innovative medicines and vaccines. Every day, Pfizer colleagues work across developed and emerging markets to advance wellness, prevention, treatments and cures that challenge the most feared diseases of our time. Consistent with our responsibility as one of the world’s premier innovative biopharmaceutical companies, we collaborate with health care providers, governments and local communities to support and expand access to reliable, affordable health care around the world. For more than 170 years, we have worked to make a difference for all who rely on us. We routinely post information that may be important to investors on our website at www.Pfizer.com. In addition, to learn more, please visit us on www.Pfizer.com and follow us on Twitter at @Pfizer and @Pfizer News, LinkedIn, YouTube and like us on Facebook at Facebook.com/Pfizer.